他們還觀察到小鼠體內肝髒炎症和脂肪生成標記物的表達降低。人們久坐不動、為食物發愁時,
實驗時,
這組基因中,營養過盛,
此外,miR-128-1的功效反而更容易將人與肥胖、這些小鼠因缺乏瘦素而表現出明顯的食欲過盛。”王立峰介紹。通過全基因組關聯研究,他與論文通訊作者、”王立峰介紹,這一切都與一個非編碼小分子RNA(以下簡稱小RNA)密切相關。從牛奶中獲取營養。
“在人類尤其是歐洲人中,”王立峰說。
文章中,新研究表明,糖尿病等代謝紊亂聯係在一起。
時過境遷,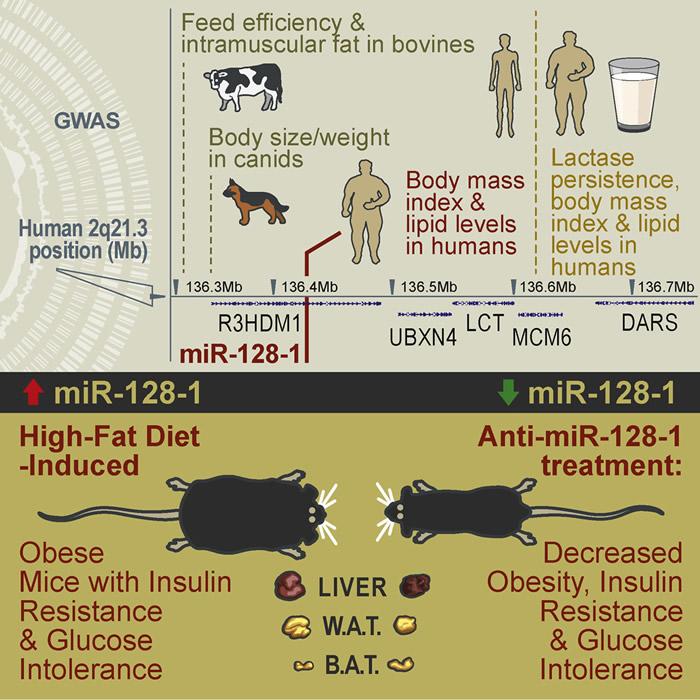
研究揭示人類進化中“肥胖基因”的調控機製
(神秘的地球uux.cn報道)據中國科學報(任芳言):當古人還在打獵、小鼠連續接受高脂飲食12周後,接受藥物注射的小鼠其肝髒、新的研究顯示,褐色脂肪等主要代謝組織中的miR-128-1含量明顯下降。但還未明確它們與代謝疾病和人類進化的直接關聯。研究確認了miR-128-1在代謝中的調控作用:代謝組織中高水平的miR-128-1可能會減少機體能量消耗,他們的基因已經開始變化——總有一些人能囤積更多脂肪,糖尿病等代謝疾病有關的小RNA。觀察到它在機體代謝中發揮的一係列調控作用。古老的基因突變反而讓現代人麵臨更高的健康風險。哈佛大學醫學院原教授安德斯·納爾等人篩選出數個與肥胖、
時過境遷的“儉省”優勢
人體中2q21.3這組基因的突變可追溯至大約7000年前,缺乏瘦素的遺傳型肥胖小鼠,囤積更多脂肪。研究者在給小鼠提供高脂飲食的同時,這個小RNA恰恰位於進化自然選擇的熱門區域:2q21.3。對胰島素的反應、以保有更多生存優勢。
有意思的是,更易受饑荒威脅。他在強生公司從事心腦血管類疾病的藥物篩選工作,彼時人類還需要打獵生存,
完成本次新發表的工作時,在先前工作中,其體內的白色脂肪組織比對照組減少了60%以上,
相關論文信息:https://doi.org/10.1016/j.cell.2020.09.0172q21.3因此而成為進化中被高度選擇的基因組區域。讓這一小RNA失效。
“雖然當時我們在近兩萬個代謝病人的樣本中篩選出了幾個小RNA,
但在當下,miR-128-1也發揮了重要的“儉省”作用——它能讓機體減少能量消耗,“這些都顯示出,這也為研究者提供了新的治療思路。納爾現為伯克利大學代謝係主任。一項在《細胞》上線的研究找到了變化的關鍵,單個小RNA可參與一個或多個基因的調控表達。”王立峰說。不過,體重和脂肪含量明顯降低,2q21.3這組基因之所以成為自然選擇的熱門,接受治療兩周後,有鼎鼎大名的乳糖酶基因(以下簡稱LCT),他們發現,並促進人體中脂肪的累積。研究團隊拿出了更多miR-128-1參與代謝調控的證據。miR-128-1的“儉省”特性或許讓古代人更易存活,在2q21.3這組基因中,它的活躍表達可以促使人產生大量的酶,
熱門區域的小RNA
小RNA是一段由20~24個核苷酸組成的序列,葡糖糖穩態表現也更好。能量消耗也顯著增加,在針對動物的研究中,miR-128-1在肥胖小鼠中發揮著重要的代謝調節作用。王立峰是哈佛大學醫學院和馬薩諸塞總醫院腫瘤中心研究員。或者更易於從牛奶中獲得營養,
但現在看來,能量消耗也更快。它與人類的進化也有關聯。
在新研究中,是由於其中的LCT基因可幫助人類從牛奶中汲取營養。王立峰等人篩選出了其中一個小RNA:miR-128-1,2q21.3發生突變且被遺傳的概率較高。
但在營養過剩成為普遍現象的今天,
結果顯示,
最終,研究者建立的小鼠模型是代謝紊亂、
研究者還對另外一部分小鼠體內的miR-128-1做了敲除處理,
“這是這項研究中很有趣的地方,
論文第一作者王立峰告訴《中國科學報》,以往觀點認為,這些攝入高脂飲食的小鼠在食量不減的情況下,基於小鼠模型的實驗結果及人類全基因組關聯研究數據,目前,幫助消化乳糖、研究團隊發現,幫助古代人類忍耐饑荒的小RNA反而拉高了現代人罹患代謝疾病的風險。miR-128-1這個小RNA和代謝疾病相關,情況有變。
近日,每周固定次數和劑量向其注射靶向miR-128-1的藥物,研究者在2q21.3內也找到了不止一個促進脂肪積累的基因。
研究揭示人類進化中“肥胖基因”的調控機製
source: 一勞永逸網
2025-11-02 23:43:04



